화학1 2단원 원자의 세계 기말고사 기출문제 풀이-2
화학1 기말고사 기출문제 풀이입니다. 기말고사 범위가 보통 2단원인 원자의 세계이죠? 학교마다 다를 수 있겠지만..그래서 2단원 학교 기출문제를 가지고 풀이를 하도록 하겠습니다. 참고로 풀이를 보면 답이 보이므로, 정답은 안 적어요^^
원자 반지름
풀이과정
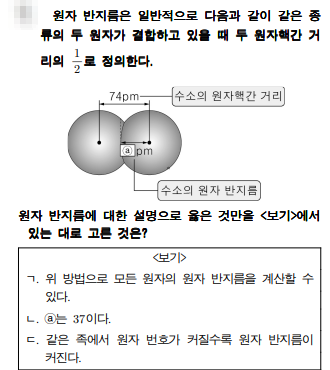
이번 문제는 원자반지름에 대한 문제입니다. 원자반지름을 구하기는 쉽지는 않죠. 보통 두 원자가 결합하고 있을 때 두 원자핵간의 1/2를 원자반지름이라고 합니다. 그림은 수소원자간의 핵간 거리가 74pm이네요. 그러면 수소원자 반지름은 74pm의 1/2인 37pm이 되네요. 원자반지름은 같은 족에서 원자번호가 커지면 전자껍질이 증가하기 때문에 원자반지름이 커지는 경향이 있군요. 같은 주기에서는 전자껍질수는 같지만, 원자번호가 클수록 유효핵전하가 커지므로 원자반지름이 작아지는 경향이 됩니다. 그럼, 이와 같은 방법으로 모든 원자의 원자반지름을 구할 수 있을까요? 비활성기체인 헬륨이나 네온은 단원자 분자이죠. 이런 경우는 결합을 하지 않기 때문에 저 방법외인 반데르발스 반지름을 이용합니다.
원자 또는 이온 반지름 비교

풀이과정
원자의 반지름은 같은 족에서는 원자번호가 클수록 커지고, 같은 주기에서는 원자번호가 클수록 작아지는 경향이 있죠. 이온반지름은 전자껍질과 유효핵전하등 여러가지를 봐야 하는데요,
Cl^-(염화이온)과 K^+(칼륨이온)은 보면 염화이온과 칼륨이온의 전자수는 18개로 같습니다. 전자수가 같으면 전자껍질의 수가 같다는 것이죠. 두 번째, 유효핵전하를 봐야 하는데요, 염화이온의 양성자수는 17개이고, 칼륨이온은 19개입니다. 따라서 유효핵전하는 칼륨이온이 크죠. 그러면 전자를 더 많이 잡아당기므로, 이온반지름은 칼륨이온이 염화이온보다 조금 작습니다.
두 번째, 리튬이온과 리튬원자네요. 양성자수는 같죠. 근데, 전자수는 리튬이온이 하나 적어요. 그러면 전자껍질수를 비교하면 리튬이온은 1개이고, 리튬원자는 2개이므로 리튬이온의 반지름이 작네요.
세 번째, 마그네슘과 칼슘입니다. 같은 족이네요. 원자번호는 칼슘이 크죠. 그리고 전자수도 칼슘이 많죠. 따라서, 전자수가 많은 칼슘의 원자반지름이 마그네슘보다 크죠.
주기율표

풀이과정
현대의 주기율표는 영국의 물리학자인 모즐린에 의해서 발표한 것을 사용하고 있습니다. 모즐린은 X 선 연구를 통해서 원자들의 양성자수를 순서대로 배열하였는데, 이 양성자수가 바로 원자번호입니다. 모즐린의 주기율표가 나오기 전까지는 러시아의 화학자인 멘델레예프가 발표한 주기율표를 사용했는데요, 불편한 점이 없지는 않았죠.
ㄱ. 1족에 속하는 원소에는 수소, 리튬, 나트륨, 칼륨이 있는데요, 수소를 제외하고는 모든 금속원소입니다. 따라서 수소를 제외하고는 화학적 성질이 비슷하죠.
ㄴ. 2주기에는 리튬, 베릴륨, 붕소, 탄소, 질소, 산소, 플루오린, 네온으로 총 8개의 원소가 들어 있죠.
ㄷ. 원자량 순서대로 만든 주기율표는 멘델레예프가 고안한 것이예요^^
원소의 주기적 성질

풀이과정
주기율표에는 원소마다 성질이 다르겠지만, 비슷한 성질이 있죠. 이를 원소의 주기적 성질이라고 합니다.
유효핵전하란 내부의 전자들이 원자핵을 가려막으면서 생기는 실제로 전자들이 느끼는 핵전하입니다. 같은 주기에서 유효핵전하는 원자번호가 클수록 증가하는데요, 이는 원자번호가 증가하면 양성자수도 증가하고, 전자껍질에 전자도 증가하지만, 증가한 전자가 원자핵으로부터 완전히 가려지지도 않기 때문에 일반적으로 유효핵전하는 증가합니다.
이온화에너지는 가장 바깥쪽에 있는 전자껍질에서 전자 한 개를 떼어낼 때 필요한 에너지입니다. 그럼 원자핵과 멀리 있을수록 쉽게 떼어낼 수 있겠네요? 따라서 같은 주기에서 원자번호가 증가하면 유효핵전하가 증가하기 때문에 전자를 떼어낼 때 많은 에너지가 필요하죠. 모든 원자에서 가장 이온화에너지가 큰 원자는 헬륨입니다. 왜? 전자껍질이 한개이고, 전자껍질에는 전자 2개만 들어 갈 수 있죠. 그리고 원자핵과 다른 원자에 비해서 아주 가까워요. 따라서 이온화에너지가 가장 큰 원자는 헬륨입니다.
양자수
풀이과정
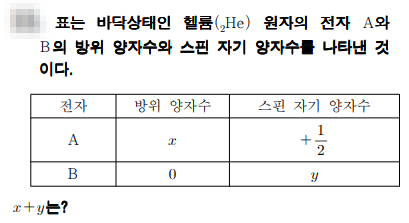
양자수는 원자안에 있는 전자들을 양자화하여 나타낸 수를 말하죠. 주양자수, 방위(부)양자수, 자기 양자수, 스핀자기 양자수 이렇게 있죠. 방위양자수는 0부터 주양자수 -1 하면 되고, 스핀자기 양자수는 +1/2와 -1/2로 되어 있습니다. 참고 두전자의 양자수에서 주양자수, 방위양자수, 자기 양자수까지는 같을 수 있지만, 스핀 자기 양자수만은 무조건 달라야 해요. (파울리베타원리 위배)
헬륨은 주 양자수는 1이죠. 따라서 방위양자수는 0입니다. 그리고 전자가 두개 있으니까, 스핀 양자수는 +1/2 또는 -1/2 이겠죠? 답 보이시나요??
이상 화학1 기말고사 대비 기출문제로 몇문제 풀어봤습니다.
구독과 하트, 광고는 제게 큰 도움이 됩니다.^^
