23년 3월 모의고사 문제 및 해설-1
어제 3월 모의고사 학생들이 봤습니다. 제 아이들은 아직 어려서.... 많이 기다려야 하지만... 다들 좋은 성과가 있었으면 합니다. 문제풀이 해볼까요??
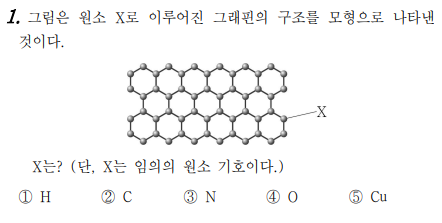
1번 문제는 탄소 동소체에 대한 문제입니다. 그래핀은 탄소들이 육각형으로 이루어진 구조물입니다. 동소체란 구성하는 원소는 같은데, 성질이 다른 여러 가지 물질을 말합니다. 동소체에 대표가 탄소인데요, 탄소 동소체에는 다이아몬도, 흑연, 그래핀, 탄소나노튜브등이 있고, 모두 C로 표현합니다.

2번 문제는 실생활에서 화학이 어떻게 사용되는가에 대한 문제입니다. 암모니아는 질소비료를 만들수 있는 계기가 되었죠. 그리고 최초의 합성 섬유는 나일론입니다. 나일론은 탄소화합물이지만, 암모니아의 화학식은 NH3으로 탄소화합물이 아닙니다.

3번 문제는 탄소화합물의 성질이네요. 식초의 주성분은 아세트산이고요, 손 소독제로 사용하는 물질은 에탄올이죠. 그리고 연료로 사용되는 물질은 메테인입니다. 집에서 사용하는 연료로는 도시가스(천연가스)와 LPG 가스가 있죠. 도시가스에서 사용하는 것이 메테인이고요, LPG은 프로판 가스를 말합니다.
아세트산은 물속에서 수소이온과 아세트산이온으로 이온화가 약하게 일어나므로 산으로 작용합니다.
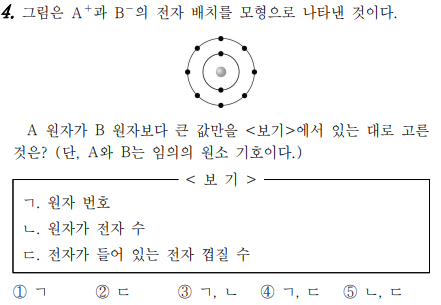
4번 문제는 원자에서 전자 배치를 정확하게 이해하는지에 대한 문제입니다. A+ 이온과 B- 이온의 전자배치가 그림과 같다면, A는 금속원소이고, B는 비금속원소네요. 그리고 원자일 때 전자수는 양이온이라면 이온일 때 전자배치에서 잃어버린 전자수만큼 더해주면 되고, 음이온이라면 이온일 때 전자배치에서 얻는 전자수만큼 빼면 원자일 때 전자수를 알 수 있습니다. A는 이온일 때 전자가 10개이네요. 그럼 원자일 때 전자는 1개를 더해주면 되니까, 11개이죠. 그럼 양성자수도 11개이고, 원자번호는 11번, 3주기에 있는 나트륨이네요. B는 이온일 때 전자가 10개이죠. 원자일 때 전자는 1개를 빼면 되므로 원자일 때 전자는 9개, 그럼 양성자수도 9개이므로 원자번호는 9번인 플루오린이죠. 2주기에 있는~~
원자가 전자수는 원자일 때 가장 바깥쪽에 있는 전자수이죠. 나트륨은 1개이고, 플루오린은 7개이죠.
정답 찾을 수 있으시죠??
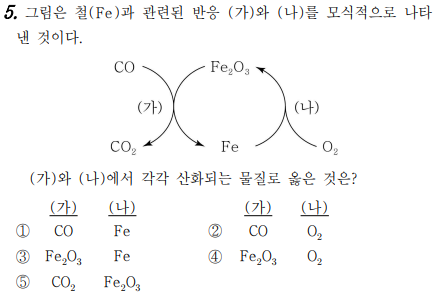
5번 문제는 산화환원에 대한 문제입니다. 산화란 산소를 얻거나, 전자를 잃어버린 것을 말하고, 환원은 산소를 잃어버리거나, 전자를 얻으면 환원이라고 하죠. 산화환원은 동시에 일어납니다.
가는 CO + Fe3O2 -> CO2 + Fe이고, 나는 Fe + O2 -> Fe3O2 이죠.
그럼 가에서 일산화탄소가 산소를 받아서 이산화탄소가 되므로 산화이고, 나에서는 철이 산소과 반응하여 산화철이 되었죠. 답 보이시죠??
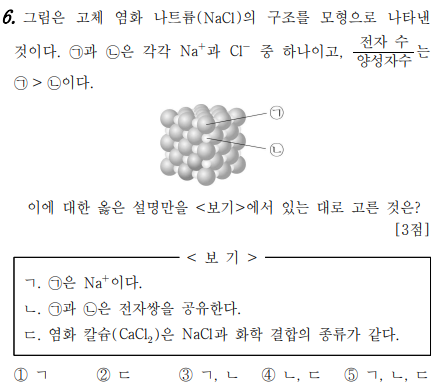
6번 문제는 이온결합에 대한 문제입니다. 염화나트륨은 나트륨이온과 염화이온이 정전기적 인력에 의해서 결합이 된 이온결합물질입니다. 우선 ㄱ과 ㄴ을 찾아야 하는데, 전자수/양성자수는 ㄱ이 ㄴ보다 크다고 했네요. 나트륨이온의 양성자수는 11개이고 전자는 10개, 염화이온은 양성자수가 17개, 전자수는 18개입니다. 그럼, ㄱ과 ㄴ 찾을 수 있죠? 염화칼슘은 염화나트륨처럼 양이온과 음이온이 정전기적 인력에 의해서 결합한 이온결합물질이에요^^
정답은 알아서 찾아보세요^^

7번 문제는 금속에 대한 성질을 물어보는 문제입니다.
리튬은 금속이죠. 이런 금속이 물에 있는 수소이온과 전자를 주고받으면서 리튬은 수소이온한테 전자를 줘서 리튬이온으로 되고, 수소이온은 전자를 얻어서 수소원자가 되고, 수소원자들 합쳐져서 수소기체가 발생합니다. 모든 금속이 수소와 반응하는 것은 아니지만, 수소보다 반응성이 큰 금속원소들에게 일어나는 현상입니다.
결과를 보면 Li 조각이 물과 격렬하게 반응하여 수소기체가 발생하였다. -> 금속 리튬은 물속에 들어가서 물 속에 있는 수소이온에게 전자를 주고 양이온이 되고, 수소이온은 전자를 받아서 수소기체가 되죠.
수용액이 붉은색으로 변하였다. - 페놀프탈레인 용액은 염기성일 때 붉은색으로 변합니다. 물속에서 물은 적지만, 수소이온과 수산화이온으로 이온화가 되므로 수소이온은 전자를 받아서 수소기체가 되고, 수산화이온은 물 속에 남게 됩니다. 이 수산화이온 때문에 염기성이 나오는 것이죠. 금속 리튬대신 나트륨으로 실험해도 결과는 같이 나와요^^
8번 문제부터는 내일 올리도록 할게요^^
구독과 하트, 광고는 제게 큰 도움이 됩니다.^^
