과외하는 두 아이의 아빠
중3 1단원 마무리 문제 (2) 본문
다섯 번째 문제입니다.

기체 반응 법칙에 관한 문제입니다.
문제를 보기 전에 표를 통해서 기체 A와 기체 B의 부피비를 알아야 하는데요, (가) 실험에서 반응 전 기체 A와 B가 각각 12, 14ml였는데, 반응 후 기체 B가 10ml 남았네요. 그럼, 반응에 참여한 기체 B의 양은 4ml이라는 것 알 수 있습니다. 따라서 기체 A와 기체 B의 부피비는 12 : 4 = 3 : 1입니다.
(나)를 통해서 생성된 부피비도 알 수 있는데요, 반응 전 기체 A와 기체 B의 양은 각각 a와 6ml 이고, 반응 후 기체 A가 2ml 남았죠. 그럼 기체 B는 전부 사용했기 때문에 부피비가 (a-2) : 6 = 3 : 1 이므로 a-2=18이 되어야 하므로 a는 20입니다. 이해가 되시나요??? 그리고 반응 후 기체 C가 12ml 생성되었으므로 기체 A : 기체 B : 기체 C의 부피비는 18 : 6 : 12 = 3 : 1 : 2입니다.
문제를 보면 기체 A 9ml와 기체 B 10ml가 반응하였을 때 생성되는 기체 C의 부피와 반응하지 않고 남는 기체의 종류와 부피라고 물어보고 있네요.
표에서 기체 A : 기체 B : 기체 C의 부피비는 3 : 1 : 2 이므로, 기체 A 9ml 다 반응하기 위해서는 기체 B는 3ml만 있으면 되네요. 그리고 생성되는 기체 C의 부피는 6ml만 만들어지네요.
여섯 번째 문제입니다.

구리를 가열하여 산화구리를 만드는 반응입니다. 표를 통해서 구리와 산소, 산화구리의 질량비를 알 수 있습니다.
실험 1에서 구리 0.4g과 산소를 반응시켰더니 산화구리 0.5g 생성되었네요. 질량 보존 법칙에 의해서 반응 전과 후 원소의 종류와 개수는 사라지지 않고, 늘 일정하므로, 산화구리가 0.5g에서 구리가 0.4g 뺀 0.1g 은 산소의 질량입니다. 따라서 구리와 산소, 산화구리의 질량비는 0.4 : 0.1 : 0.5 이므로 4 : 1 : 5입니다. 그리고 산화구리를 생성할 때 구리와 산소의 질량비는 절대로 변하지 않습니다. 왜? 일정성분비 법칙 때문인데요, 일정성분비 법칙이란 한 화합물을 생성할 때 구성하는 원소들 간의 질량비는 항상 일정하기 때문이죠. 실험 1~4번까지 구리와 산소의 질량비가 일정함을 알 수 있습니다.
그럼 정답은 뭘까요??
일곱 번째 문제입니다.
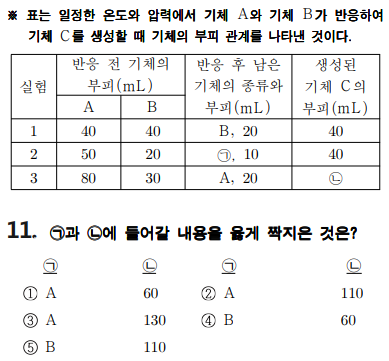
기체 A와 기체 B가 반응하여 기체 C를 생성하는 반응인데, 표를 통해서 기체 A와 기체 B, 기체 C의 부피비를 알 수 있죠.
실험 1에서 반응 전 기체 A와 기체 B의 각각 40ml, 반응 후 남은 기체 B가 20ml이므로 실제로 반응에 참여한 기체 B는 20ml이죠. 그럼 기체 A와 기체 B의 부피비는 40 : 20 = 2 : 1이네요. 그리고 생성된 기체 C의 부피가 40ml 이므로 기체 A와 기체 B, 기체 C의 부피비는 2 : 1 : 2 이죠. 부피비만 알면 쉽게 풀 수 있는 문제입니다.
정답은 직접~~~
여덟 번째 문제입니다.

화학반응이 일어날 때 열에너지가 필요한 흡열 반응과 열에너지가 방출한 발열반응으로 나눕니다. 문제는 발열반응에 해당하는 반응을 찾으라는 것인데, 특별한 팁은 없습니다. 발열반응보다 흡열반응이 적기 때문에 흡열반응의 예를 암기하던지 아니면, 전부 다 암기하는 방법 외에는.....
a) 금속과 식초의 반응 - 금속과 산의 반응입니다. 발열 반응
b) 염산과 수산화나트륨의 반응 - 산과 염기의 반응으로 중화반응입니다. 발열반응
c) 광합성할 때 이산화탄소와 물의 반응 - 광합성할 때 빛이 꼭 필요하죠? 그러면 빛에는 열도 있기 때문에 열이 필요한 반응이므로 흡열반응
d) 마그네슘 리본이 연소 반응 - 연소를 타는 것이죠? 탈 때 빛과 열이 나오므로 발열반응
e) 탄산수소나트륨의 분해 반응 - 화합물을 분해하려면 열을 공급해야 분해가 일어납니다. 열이 필요한 반응이므로 흡열반응
정답은 직접...
아홉 번째 문제입니다.
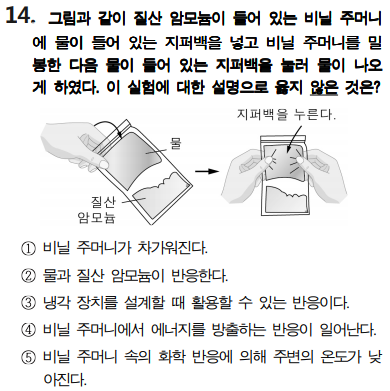
질산암모늄과 물이 반응하는 대표적인 흡열반응입니다. 지퍼백을 누르면 물과 질산암모늄이 반응하여 주변의 열을 뺏아가면서 주변의 온도가 낮아지면서 냉각장치를 설계할 때 활용하는 방안입니다. 이외에 수산화바륨과 염화암모늄 반응도 흡열 반응이죠.
그럼 정답 찾아보세요^^
1단원 총 10문제를 하려고 했는데, 각 단원에서 중요한 부분만 발췌를 하다 보니 9문제만 되었네요.. 이점 양해해 주세요^^
모르는 부분이 있으면 댓글 주시면 자세하게 설명해드리겠습니다.^^
2022.12.21 - [중등과학문제풀이/중3 과학 이론] - 중3 1단원 화학파트에서 배우는 3가지 법칙
중3 1단원 화학파트에서 배우는 3가지 법칙
안녕하세요 오늘은 본격적으로 이론에 대하여 적어볼게요. 1단원 화학에서 나오는 3가지 법칙 바로 질량 보존의 법칙, 일정성분비의 법칙, 기체 반응의 법칙입니다. 질량 보존의 법칙은 문자 그
kblue77.tistory.com
2023.01.23 - [중등과학문제풀이/중3 과학 이론] - 중3 화학반응시 에너지 출입
중3 화학반응시 에너지 출입
안녕하세요^^ 새해 복 많이 받으세요^^ 오늘은 중3 과학 1단원에 마지막 파트인 화학반응이 일어날 때 에너지 출입에 대하여 알아보겠습니다. 화학반응이 일어날 때 에너지 출입(이동)은 두 가지
kblue77.tistory.com
이론편도 링크 했으니, 꼭 읽어보시기를 바랍니다.^^
구독과 하트는 제게 큰 도움이 됩니다.^^

'중등과학문제' 카테고리의 다른 글
| 중3 2단원 마무리 문제 (2) (14) | 2023.03.02 |
|---|---|
| 중3 2단원 마무리 문제 (1) (20) | 2023.03.02 |
| 중3 1단원 마무리 문제(1) (14) | 2023.02.28 |
| 중3 반응과 항상성 문제 (14) | 2023.02.27 |
| 중3 자율신경계과 무조건 반사 문제 (17) | 2023.02.27 |





