과외하는 두 아이의 아빠
1단원- 원자와 분자 (1) 본문
- 물질을 구성하는 입자 -
물질을 구성하는 입자가 원자라는 것을 알아낸 것은 언제부터일까요? 지금이 21세기이죠? 입자가 원자라는 것을 알아낸 것은 17세기 이에요. 약 400년 정도 되었네요. 생각보다 짧은 역사를 가지고 있다는 것...
- 입자설 VS 연속설 -
물질을 구성하는 것이 무엇일까? 물질관에 대해서 이미 설명을 했는데, 고대 시대때 물질의 구성을 두고 두 학자가 열띤 토론을 했습니다 데모크리토스의 '입자설'과 아리스토텔레스의 '연속설' 이죠.
입자설은 "물질을 계속 쪼개면 언젠가는 더 이상 쪼갤 수 없는 입자로 구성되어 있고, 입자와 입자사이에는 빈 공간이 있다는 것"이고, 연속설은 "물질을 계속 쪼개면 무한히 쪼개면 언젠가는 사라질 것이다. 그리고 빈 공간은 존재하지 않는다. "는 것이죠.
하지만, 고대시대에는 물질을 계속 쪼개면 언젠가는 없어질 것이라고 믿고 있었습니다. 왜? 그 당시에 기술이 지금 하고는 많이 다르죠. 그래서 눈에 보이는 것이 전부였다고 저는 생각합니다. 아무튼 이런 연속설을 주장한 아리스토텔레는 후세의 연금술에 영향을 많이 줬죠.
| 데모크리토스의 입자설 | 아리스토텔레스의 연속설 |
 |
 |
- 하이탑 중2과학 참조 -
- 보일의 원소설 -
아리스토텔레스의 연속설을 오랜 시간동안 영향을 주었다가, 17세기에 와서 보일이란 과학자가 J자관 실험을 통해서 연속설이 틀렸다는 것을 증명합니다.
보일은 J 자관 실험을 통해서 입자와 입자 사이의 빈 공간이 있음을 증명하였습니다.
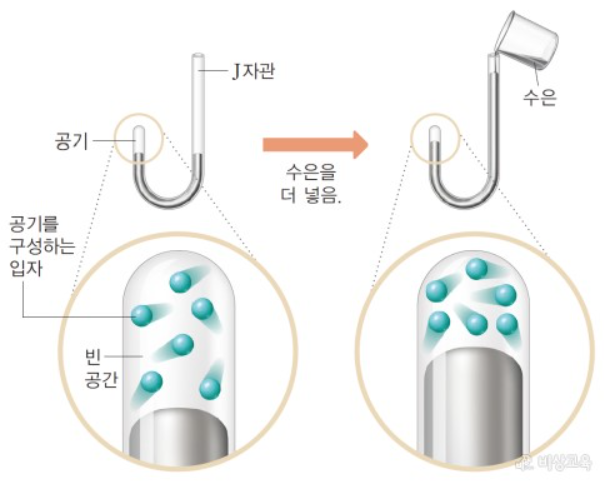
그림을 보시면 한쪽이 막힌 J자관을 준비하고, 수은을 넣었습니다. 그리고 수은을 더 넣으면 막힌 쪽의 수은이 올라가는 것을 알 수 있죠. 여기서 왜 수은을 넣으면 빈 공간이 줄어들까? 보일은 빈 공간에는 공기가 들어 있는데, 수은을 더 넣으면 공기를 구성하는 입자와 입자사이의 공간이 줄어들기 때문이라고 합니다. 그렇다면 연속설 입자에서는 어떻게 설명할까? 연속설 입장에서는 빈 공간이 줄어드는 것은 공기의 농도가 진해졌기 때문이라고 하죠. 그럼, 누가 맞을까요? 연속설에서 말하는 공기의 농도가 진해졌다? 농도라는 것을 쉽게 말하면, 공기의 양입니다. 다시 말해서 공기의 농도가 진해졌다는 것은 공기의 양이 많아졌다는 것인데, 막힌 관에서 공기가 들어갈 수 있는 공간이 있나요? 없습니다. 따라서 공기의 농도가 진해졌다고는 볼 수가 없죠. 그래서 보일은 "공기를 이루는 입자와 입자사이의 공간이 줄어들었기 때문이다."라고 하면서 연속설이 틀리고 입자설이 맞다고 이야기하면서, 물질은 입자로 구성되어 있다고 주장을 합니다.
| 입자설의 증거 |
| 1. 금속박이나 비누방울의 막을 무한히 얇게 만들 수 없다. -> 무한히 얇게 만들 수 없는 이유는 입자의 크기보다 작게 만들 수 없다는 것이다. 2. 풍선을 불어서 가만히 있으면, 풍선의 크기가 점점 작아진다. -> 풍선을 입자들 사이로 공기 입자가 빠져 나가기 때문이다. 3. 물과 에탄올을 혼합하면 전체 부피는 혼합전 부피의 합보다 작다. -> 큰 입자 사이로 작은 입자가 들어가기 때문이다. |
- 돌턴의 원자설 -
돌턴은 물질을 구성하는 가장 작은 입자를 원자라고 하고, 원자설을 제안했습니다.
| 돌턴의 원자설 | |
1. 물질은 더 이상 쪼갤 수 없는 원자로 구성되어 있다.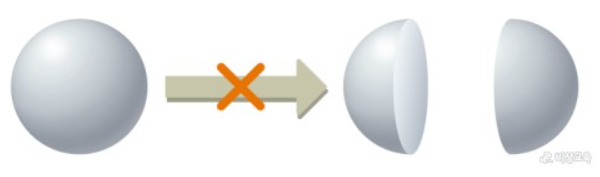 |
2. 원자의 종류가 같으면, 크기와 질량은 같고, 종류가 다르면 크기와 질량은 다르다.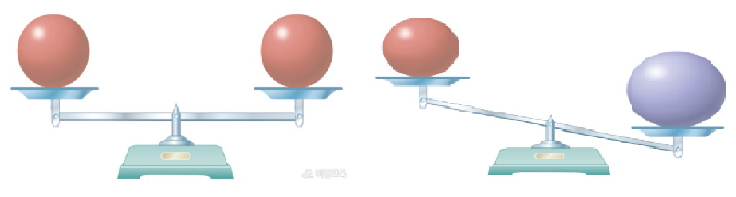 |
3. 원자는 새로 생기거나, 사라지지 않으면, 다른 원자로 변하지 않는다. |
4. 서로 다른 원자들이 일정한 비율로 결합하여 새로운 물질을 만든다. |
- 비상 교육 참조 -
현재, 돌턴의 원자설은 수정이 불가피합니다. 기술이 발전하였기 때문이죠.
1. 원자는 쪼개지지 않는다. - 원자는 원자핵과 전자로 나뉘고, 핵분열에 의해서 쪼개지지도 합니다.
2. 같은 원소라면 크기와 질량이 같다. - 동위원소라는 것이 있는데, 양성자의 수는 같아서 같은 원소이지만, 중성장의 수가 달라서 크기와 질량이 다른 원소가 발견되었습니다.
3. 원자는 새로 생기거나, 사라지지 않으며, 다른 원자로 변하지 않는다. - 핵분열에 의해서 다른 원자로 변할 수 있습니다.
- 원자 -
원자란 물질을 구성하는 가장 기본 입자를 말합니다. 입자라는 것을 알갱이로 셀 수 있는 것을 말합니다. 원소와는 다른 개념인데, 원소는 물질을 구성하는 가장 기본 성분을 말합니다. 성분이기 때문에 셀 수 없어요.
원자는 원자핵과 전자로 구성되어 있어요. 다시 원자핵은 양성자와 중성자로 구성되어 있습니다.
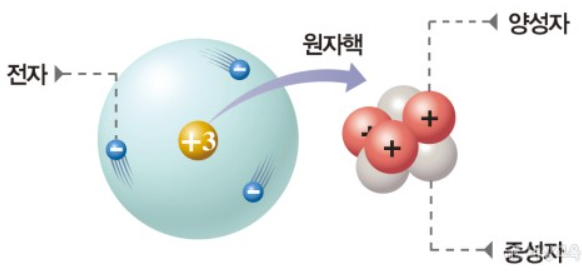
- 원자는 전기적으로 중성 -
원자는 전기적으로 중성입니다. 원자핵은 양성자와 중성자로 구성되어 있는데, 양성자는 (+) 전하량을 띠고 있고, 중성자는 중성입니다. 그리고 원자핵 주변을 돌고 있는 전자는 (-) 전하량을 띠고 있고 있습니다. 전기적으로 중성이어야 하므로, 양성자의 (+) 전하량의 총 개수와 전자의 (-) 전하량의 총 개수가 같다는 것 명심하세요^^
- 원자의 크기 -
원자의 크기는 엄청 작아요. 가장 작은 수소원자 1억개를 펼치면 어느 정도의 길이가 될까요? 그 길이는 약 1cm도 안될 정도입니다. 그렇기 때문에 육안으로 보는 것은 거의 불가능하고, 전자현미경 같은 도구를 이용해서 볼 수밖에 없습니다.
가령, 원자를 탁구공만큼 확대를 했다고 합시다. 다시 원자를 탁구공 만큼 확대한 크기로 탁구공을 확대하면 어느 정도의 크기가 될까요? 탁구공은 지구만큼의 크기가 됩니다. 엄청 작다는 것....

- 원자의 질량 -
원자의 질량은 거의 대부분 원자핵이 차지하고 있습니다. 원자핵은 양성자와 중성자로 나눈다고 했죠? 양성자와 중성자의 질량은 거의 같다고 보고 있고, 전자의 질량은 양성자에 비해서 훨씬 작아요. 약 1/1680배 정도라고 보면 됩니다.
- 원자의 전하 -
이미 앞에서 말했지만, 원자는 전기적으로 중성입니다. 양성자의 총 전하량과 전자의 총전하량이 같아서입니다.
그럼, 원자마다 양성자의 개수가 다른가요? 네. 원자마다 양성자의 수는 다릅니다. 가장 작은 수소원자는 양성자가 1개이고, 헬륨은 양성자의 개수가 2개입니다. 그리고 소금 들어봤죠? 소금은 나트륨이온과 염화이온이 합쳐져서 만들었는데, 이온은 다음 시간에 포스팅을 할 예정이에요. 일단 나트륨은 양성자의 개수가 11개, 염소는 양성자의 개수가 17개입니다. 이처럼 원자마다 양성자의 개수가 다릅니다. 그럼 전자의 개수도 다르겠죠? 원자이면 전기적으로 중성이니 양성자의 개수만큼 전자가 있다고 보면 됩니다. 수소원자는 양성자의 개수가 1개이므로 전자도 1개이고, 헬륨은 양성자의 개수가 2개 이므로 전자도 2개 있다고 보면 됩니다.

- 원자의 모형 -
원자는 눈에 보이지 않을 만큼 작다고 했죠. 그래서 우리는 원자를 모형으로 가지고 원자의 성질을 이해하거나 쉽게 설명합니다.

지금까지 원자에 대한 포스팅이었습니다. 조금 있다가 분자에 대한 포스팅 하도록 하겠습니다.^^
구독과 하트, 광고는 제게 큰 도움이 됩니다.^^

'중등과학문제 > 중2 과학이론' 카테고리의 다른 글
| 1단원 - 화학식(분자식), 이온 (30) | 2023.03.27 |
|---|---|
| 1단원 - 원소 기호 (14) | 2023.03.27 |
| 1단원 - 원자와 분자(2) (29) | 2023.03.26 |
| 1단원 - 원소 (2) (22) | 2023.03.11 |
| 중2 과학 1단원 - 원소(고대~근대까지 물질관)1 (26) | 2023.03.09 |





